CuMn2O4 催化臭氧氧化实验材料与方法
近年来,由于高级氧化技术可以产生大量活性氧组分 (ROS,如·OH、 SO4、1O2 等),从而有效促进痕量微污染物的降解,故而该技术成为降解高风险微量有机物的重要手段,而且逐渐成为研究热点。虽然单一的臭氧氧化法能有效去除不饱和芳香族和脂肪族化合物,但其对饱和有机化合物的去除率很低。为了高效去除难降解的饱和的持久性有机污染物,本文通过选用一种高性能的催化剂催化臭氧产生更多的活性物质,以达到彻底去除污染物的目的。
锰酸铜(CuMn2O4) 尖晶石是一种密度较大的空心六面体,其晶体结构主要是由Mn4+与Cu2+搭建的,还有较少的Mn3+与Cu+增加了结构的缺陷程度。CuMn2O4 可以催化臭氧产生具有氧化能力强、无选择性的·OH,从而有效提高臭氧对水体中难降解污染物的去除效果。有研究指出,臭氧与CuMn2O4 的结合对二苯甲酮-3 的降解有明显的协同作用。然而, 在实际使用过程中,CuMn2O4 的密度大、容易团聚、不易分散的特性使其利用率很低。为了提高其利用率,需要选用另外一种催化剂进行耦合,弥补其在使用过程中的缺陷。研究表明,二维层状碳材料在催化臭氧氧化领域中有很好的效果。因为二维层状碳材料不仅在平面内的热运输和电荷运输过程中具有突出的物理化学特性,而且与其他材料复合后可以产生良好的耦合效应。石墨烯/还原氧化石墨烯(rGO) 是其中一种极具吸引力的二维材料,具有卓越的化学稳定性、导电性和表面体积比。
此外,石墨相氮化碳(g-C3N4) 是一种具有2.7 eV 带隙的二维非金属聚合物半导体,在化学、热和光照射过程中具有较好的稳定性。同时,g-C3N4 还是一种有效的催化剂载体,在其中掺杂选定的杂原子, 通过电荷转移可以形成络合的复合材料。因此, 可以考虑将rGO 和g-C3N4 与CuMn2O4 进行复合,应用于催化臭氧氧化过程中。与大多数亲脂性的有机防晒剂不同的是,二苯甲酮-4(BP-4) 是一种亲水性的紫外线吸收剂,因其质地更轻、油性更少,被广泛应用于洗发水、剃须凝胶、止汗剂、化妆品和牙膏等日用品中。但是,由于BP-4 化学稳定性好、不易降解,因而被认为是一种伪持久性有机污染物,越来越受到人们的关注。在目前的废水处理领域中常见的水处理方法并不能将其完全去除。此外,由于rGO 和g-C3N4 在催化臭氧氧化过程中对臭氧氧化副产物溴酸盐有很好的抑制效果,因此,本研究将rGO 和g-C3N4 与CuMn2O4 复合,来探究他们在催化臭氧氧化过程中对BP-4 的降解效果以及溴酸盐生成的影响。
1 材料与方法
1.1 实验原料及仪器
一水合硫酸锰(MnSO4·H2O,≥99.0%)、三水合硝酸铜(Cu(NO3)2·3H2O,≥99.0%)、碳酸钠(Na2CO3,≥99.8%)、尿素(CO(NH2)2,99%)、硝酸钠(NaNO3,≥99.0%)、高锰酸钾(KMnO4,≥99.0%)、二苯甲酮-4(C14H12O6S,98%)、硫酸(H2SO4,≥70%)、石墨粉、过氧化氢(H2O2,≥27.5%) 和盐酸(HCl,38%)。
X 射线衍射仪;比表面积测试仪;X 射线光电子能谱仪;高效液相色谱仪;智能箱式高温炉;恒温水浴振荡器;鼓风干燥箱;电子天平;pH 计;离子色谱仪;电化学工作站;磁力搅拌器;电子扫描显微镜。
1.2 实验装置
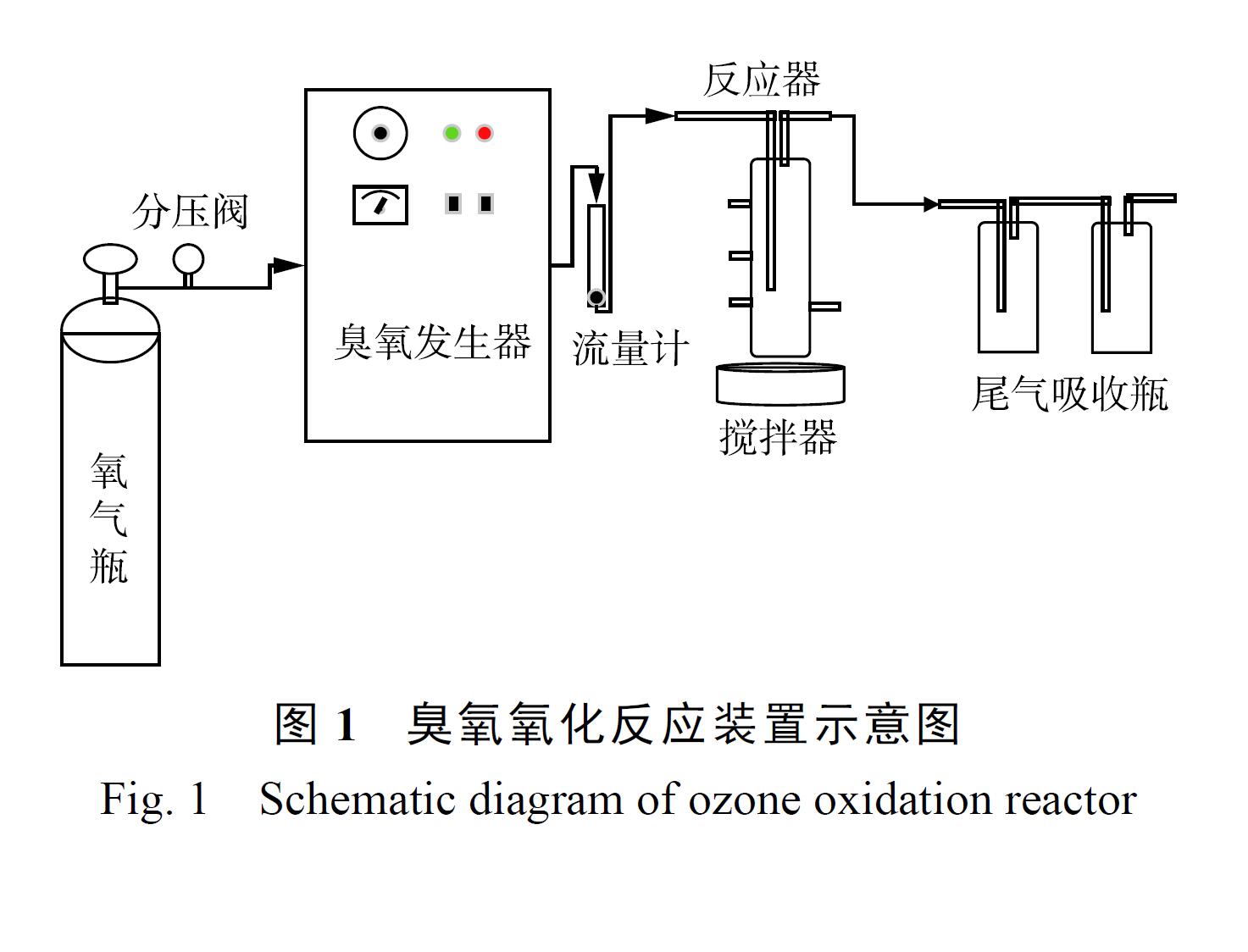
催化臭氧氧化BP-4 的效能实验采用间歇反应模式进行。反应器为圆柱形的玻璃容器,直径为6.2 cm,高为26.5 cm,有效容积为300 mL。实验使用北京同林科技有限公司生产的
3S-A5 型臭氧发生器(臭氧产量为0~1 g·h−1),以高纯氧气为气源,本实验所用的实验装置如图1 所示。实验中每次处理的水样为300 mL,所有的溶液均用去离子水配制。臭氧进气浓度通过臭氧发生器的放电功率来调节。在每次实验开始之前,用纯氧进行吹扫,并预臭氧化处理。打开臭氧发生器, 调节气流量为400mL·min−1,臭氧发生器电流为0.025 A,预热时间为60 min,预臭氧时间为30 min。
1.3 实验方法
在反应器中加入290 mL 超纯水,O3 曝气30 min,搅拌器的转速为800 r·min−1。加入10 mL BP-4母液(反应器中的浓度是0.084 mmol·L−1(25.91 mg·L−1));100 μL Br−母液(母液浓度为300 mg·L−1,反应器中的浓度是100 μg·L−1),开始反应并计时。在反应时间为0、1、2、5、7、10、15、30 min 时分别取样,并使用浓度为10 mmol·L−1 的亚硫酸钠溶液还原残留臭氧;使用0.22 μm 的水系滤膜过滤粉体催化剂后待分析。
1.4 分析方法
使用X-射线衍射仪(XRD) 对制得的粉体催化剂的矿物组成与结晶结构进行分析;使用比表面积分析仪对制得的粉末催化剂的比表面积及表面孔结构进行表征; 使用X 射线光电子能谱仪(XPS) 表征粉末状催化剂中各元素的价态;使用电化学工作站分析粉末催化剂的阻抗。使用扫描电镜(SEM) 对制得的粉末催化剂进行表观形貌的分析。
2结论
2.1使用两步煅烧法成功制备出了CuMn2O4/rGO 与CuMn2O4/g-C3N4。通过XRD 表征、BET 比表面积分析、XPS 分析以及电化学交流阻抗测试分析发现,尽管CuMn2O4/g-C3N4 比CuMn2O4/rGO 电子转移速率更快、氧空位更多,但是CuMn2O4/rGO 比CuMn2O4/g-C3N4 的结晶度更高、比表面积更大、导电性更好。
2.2 通过催化臭氧氧化降解BP-4 的实验结果表明,rGO 和g-C3N4 的掺入均能有效提升CuMn2O4催化臭氧氧化降解BP-4 的速率。但是,二者的掺入对于溴酸盐生成的控制效果有显著差异。在掺入rGO 后,溴酸盐的生成量能进一步减少;而g-C3N4 的掺入对溴酸盐生成的控制效果没有提升。
2.3进一步比较CuMn2O4/rGO 与CuMn2O4/g-C3N4 的结构和性能发现,rGO 和g-C3N4 掺入CuMn2O4后可以阻碍了CuMn2O4 的团聚的同时,还可以作为一个高导电性的框架,促进CuMn2O4 在催化臭氧氧化过程中电子的转移,此外,由于其具有高导电性和大表面积而提高了催化效率。综合考虑2种复合催化剂对BP-4 的降解效果与对溴酸盐的控制效果,CuMn2O4/rGO 更适用于催化臭氧氧化。